
Polykondensation am Beispiel von Polyamid
Geräte und Chemikalien:
Glasstab, 2 Bechergläser, Pinzette, Pipette, destilliertes Wasser, Universalindikator-Papier, Hexamethylendiamin, Sebacinsäuredichlorid, Heptan
Versuchsaufbau:
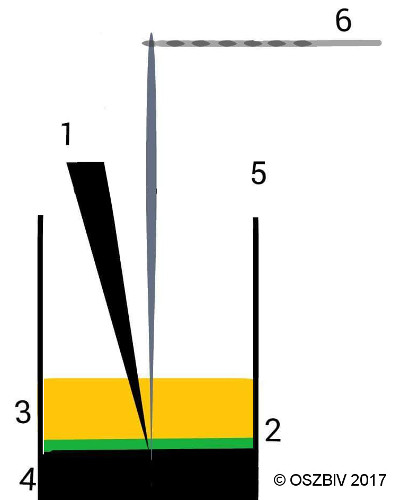
Versuchsaufbau Polyamidherstellung, Zeichnung von Hülya
1.)Pinzette, 2.)Grenzfläche, 3.)Heptan + Sebacinsäuredichlorid, 4.)Dest. Wasser + Hexanmethylendiamin, 5.)Becherglas, 6.)Glasstab
Versuchsdurchführung:
25 ml Wasser in Becherglas(1) geben und 20 ml Hexanmethylendiamin hinzugeben.
25 ml Heptan in Becherglas(2) geben und 20 ml Sebacinsäuredichlorid hinzugeben.
Vorsichtig die Lösung aus Becherglas(2) zu der Lösung in Becherglas(1) schütten, sodass sie sich überschichten
Das befeuchtete Indikator-Papier in den Dampf halten
Mit der Pinzette in die Grenzfläche greifen und einen Faden aufwickeln.
Versuchsbeobachtung:
Video aus einem anderen Kurs.
Versuchsvideo von H. X.

Reaktionn zum Polyamid, Foto von Hülya
Es bilden sich zwei Schichten.
Das Becherglas erwärmt sich.
Es bildet sich weißer Nebel.
Das Indikator-Papier färbt sich rot.
An der Grenzfläche entsteht eine weiße Haut.
Ein weißer Faden lässt sich aufrollen.
Versuchserklärung:
Es hat eine Exotherme Reaktion zwischen Hexamethylendiamin und Sebacinsäuredichlorid statt gefunden.
Die beiden Monomere werden jeweils in Lösungen gebracht, die sich nicht vermischen (Wasser und Heptan). Dadurch treffen die beiden
Monomere nur an der Grenzfläche aufeinander. Aus diesem Grund nennt man diese Reaktion Grenzflächenkondensation.
Zuerst entsteht nur ein Diamid, in dem die beiden Monomere über eine Amidbindung miteinander verknüpft sind.
Dabei wird von der Aminogruppe des Hexamethylendiamids ein Proton abgegeben, das sich mit einem Chloridion des
Sebacinsäuredichlorids zu Chlorwasserstoffgas verbindet (grün eingezeichnet).
Für Interessierte: Die Reaktionsmechanismus ist aber etwas komplzierter.
Zuerst greift das Stickstoffatom am positivierten Kohlenstoffatom der funtionellen Gruppe der Sebacinsäure an. Anschließend
finden Verschiebungen der Elektronenpaare statt, die einerseits zur Abspaltung des Protons vom Stickstoffatom und andererseits zur Abspaltung des
Chloridions vom Kohlenstoffatom führen. Diese beiden Ionen verbinden sich zu Chlorwasserstoffgas.
Das Chlorwasserstoffgas bildet mit der Feuchtigkeit der Luft
Salzsäure, die den weißen Nebel bildet.
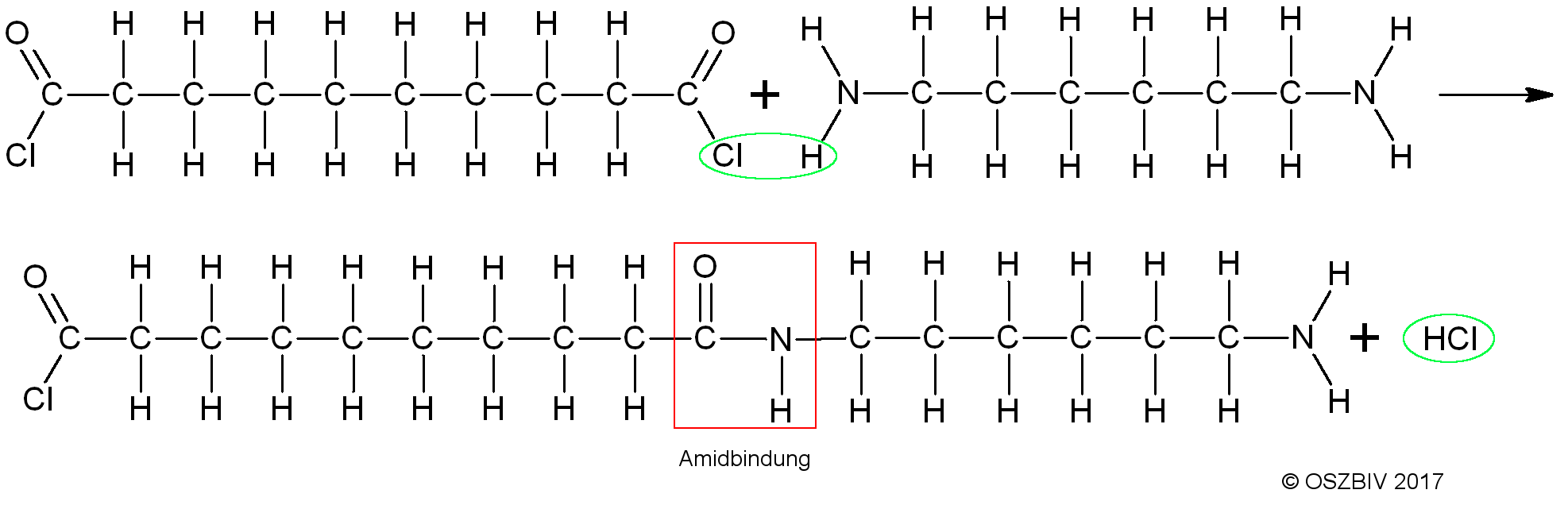
Reaktion von Sebacinsäuredichlorid (links) und Hexamethylendiamid (rechts) zum Diamid
Am Anfang und am Ende des Gebildeten Diamid-Moleküls befinden sich jeweils die funktionellen Gruppen, über die die Reaktion mit weiteren Monomeren weiter verlaufen kann. Dabei bildet sich dann das Polyamid.
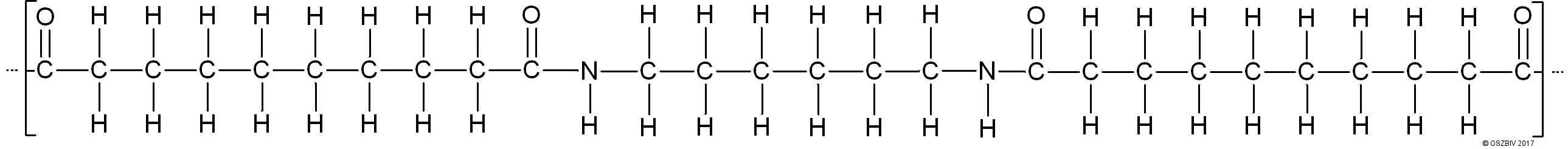
Ausschnitt aus dem Polyamidmolekül oder Nylon 6,10
Dieses Polyamid wird auch als Nylon 6,10 bezeichnet. Die 6 steht für die Anzahl der Kohlenstoffatome des Monomers Hexamthylendiamid und die 10 für die des Sebacinsäuredichlorids.
Bei dieser Reaktion reagieren zwei Monomere mit jeweils 2 funktionellen Gruppen unter Abspaltung eines kleinen Moleküls miteinander, so dass es sich um eine Polykondensation handelt.
Text erstellt von Hülya, mit kleinen Veränderungen und Ergänzungen durch Herrn Ecker 18.3.17